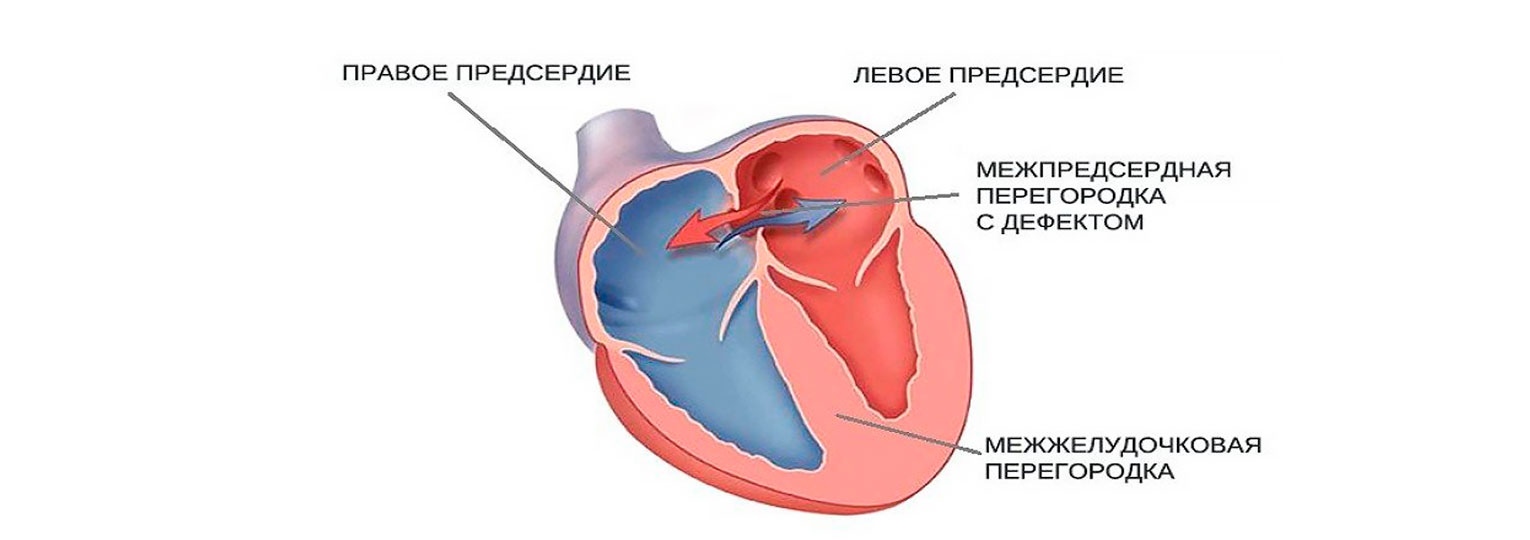
Открытое овальное окно (PFO) является распространенной аномалией сердца с распространенностью 25% в общей популяции. PFO было связано с парадоксальной эмболией, вызывающей криптогенный инсульт и системную эмболизацию. Результаты клинических испытаний, метаанализов и аналитических докладов поддерживают чрескожное закрытие PFO устройством (PPFOC), особенно если сосуществуют аневризмы межпредсердной перегородки и при наличии больших шунтов у молодых пациентов. Примечательно, что точная оценка пациентов для направления на стратегию закрытия чрезвычайно важна. Однако отбор пациентов для закрытия PFO все еще не столь ясен. Цель этого обзора — обновить и прояснить, каких пациентов следует рассматривать для лечения с помощью закрытия.
1. Введение
Открытое овальное окно (ООО) — врожденная сердечная аномалия, обычно обнаруживаемая случайно. Сообщается о частоте возникновения 20–30% в общей популяции. Примечательно, что это может быть связано с другими патологическими состояниями, такими как криптогенный инсульт (КИ), декомпрессионная болезнь (ДКБ), вторичная мигрень (ВМГ)], артериальная деоксигенация, которые были определены как синдромы, связанные с ООО. Стоит отметить, что треть ишемических инсультов считаются криптогенными, и большинство из них, как полагают, вызваны парадоксальной эмболией из-за ООО.
В ранних исследованиях превосходство интервенционной стратегии над медикаментозной терапией не было подтверждено. Однако совсем недавно было высказано предположение, что чрескожное закрытие PFO (PPFOC) с использованием новейших устройств играет значительную роль в снижении клинических событий. Согласно последним международным рекомендациям, закрытие PFO и долгосрочная антиагрегантная терапия вместо антитромботической терапии должны быть рекомендованы пациентам в возрасте от 18 до 60 лет с предыдущим инсультом или транзиторной ишемической атакой (ТИА).
Однако крайне важно выбрать тех, кто действительно может получить пользу от интервенционного подхода.
Целью данного обзора является более четкое определение того, каким пациентам следует проводить окклюзионную терапию с использованием многопараметрического подхода.
2. Эпидемиология и классификация
Криптогенный механизм, по-видимому, участвует в 10–40% всех ишемических инсультов.
Считается, что PFO вызывает около 50% криптогенных инсультов. Тем не менее, в патогенезе ишемического события могут участвовать и другие причины, такие как субклинический атеросклероз, нестабильные бляшки во внутричерепных и каротидных сосудах, артериальная диссекция, васкулит, гиперкоагуляционные состояния, другие кардиоэмболические источники и фибрилляция предсердий (ФП).
Ишемический инсульт можно классифицировать по классификации TOAST, системе фенотипирования ASCOD (A: атеросклероз; S: заболевание мелких сосудов; C: патология сердца; O: другая причина; D: диссекция) и системе классификации причин . Если полное диагностическое обследование исключает другие этиологии, инсульт можно считать криптогенным. Кроме того, КИ можно классифицировать как неэмболический или эмболический. Определение эмболического инсульта неустановленного источника (ESUS) включает нелакунарные инфаркты мозга без проксимального артериального стеноза или крупных кардиоэмболических источников. Парадоксальная тромбоэмболия связана не только с PFO, но и с AF, гиперкоагуляцией, антифосфолипидным синдромом, раком и небольшими эмболическими источниками. Также было показано, что легочная фистула подчеркивае КИ . В отличие от событий, вызванных AF, инсульты, связанные с PFO (ООО), вероятно, рентгенологически проявляются как единичное корковое поражение или как многочисленные небольшие локализованные повреждения, в основном расположенные в вертебробазилярных областях. Недавно были обновлены классификации причинных механизмов инсульта, общая номенклатура и классификация инсульта, связанного с PFO (ООО). Также был представлен точный пересмотр основных алгоритмов подтипирования инсульта. Термин «инсульт, связанный с PFO», был предложен для обозначения отдельного причинного механизма ишемического инсульта, который может использоваться после всестороннего обследования пациента . Если поверхностные, большие, глубокие или ретинальные инфаркты возникают у пациентов с PFO среднего или высокого риска без других продемонстрированных причинных факторов, мы можем назвать событие инсультом, связанным с PFO (открытым овальным окном).
3. Визуализационная оценка предполагаемой парадоксальной эмболии
Эхокардиография играет важную роль в выявлении анатомических и функциональных аспектов PFO. Трансторакальная эхокардиография (ЭХОКГ) представляет собой первый диагностический шаг для выявления ООО (открытое овальное окно) . Примечательно, что ее чувствительность низкая (46%); однако она значительно увеличивается, если выполняется гармоническая визуализация. Более того, если используется контрастный препарат с перемешиваемым физиологическим раствором , ее точность в выявлении парадоксальных шунтов справа налево из-за PFO и оценке остаточных шунтов после PPFOC значительно улучшается.
Провокационные маневры полезны для демонстрации преходящих необнаруженных парадоксальных шунтов.
Хорошо известно, что чреспищеводная эхокардиография (ЧПЭ) позволяет точно определить открытое овальное окно, оценить размер шунта, охарактеризовать анатомические особенности и провести дифференциальную диагностику с другими состояниями, такими как дефект межпредсердной перегородки , а также с источниками тромбоэмболии (сложные аортальные бляшки, фиброэластома или клапанные вегетации).
Транскраниальная допплерография (ТКД) с пузырьковым исследованием( Баббл-тест) показала свою эффективность в выявлении наличия шунтирования справа налево и, следовательно, в косвенной демонстрации PFO ( ООО). Примечательно, что если ТКД ( транскраниальная допплерография ) отрицательна, то никаких дополнительных исследований не требуется.
Логарифмическая шкала Спенсера использовалась для оценки тяжести шунтирования , классифицируя пять степеней (0–5) от отсутствия шунта (0) до тяжелого шунта (5). Степень ≥ 3, согласно шкале Спенсера, считается диагностической . Тем не менее, хотя она имеет более высокую чувствительность (97%), она ограничена в различении сердечного и легочного шунтирования, что приводит к более низкой специфичности (93%).
Первоначальная оценка с помощью транскраниальной допплерографии, а затем выполнение ЧПЭхоКГ при необходимости, является широко распространенным подходом. Действительно, положительный результат этого теста не позволяет нам точно определить, происходит ли шунтирование из-за PFO или дефекта межпредсердной перегородки, или оно является внутрилегочным.
Подход с использованием трехмерной эхокардиографии (3DE) TEE обеспечивает более полную морфологическую оценку по сравнению с TTE; кроме того, он может предоставить дополнительную информацию, которая полезна при выборе между чрескожным транскатетером и хирургическим закрытием, например, размер PFO (ООО) и точное местоположение шунтирования. Наконец, для более точного обнаружения PFO можно использовать комбинированную визуализацию. Ангиография не показана для диагностики PFO, за исключением случаев, когда она выполняется по другим причинам.
МРТ сердца реже используется для выявления ПФО из-за его низкой чувствительности.
Транскраниальная допплерография (ТКД)
Транскраниальная допплеровская ультрасонография (ТКД) является широко доступным и надежным инструментом для скрининга шунта справа налево у пациентов с инсультом. Обнаружение ТКД шунтирования справа налево должно быть дополнительно исследовано с помощью ЧПЭ для выявления признаков ООО с высоким риском. По сравнению с ЧПЭ чувствительность и специфичность ТКД для диагностики ООО составила 94% и 92% в метаанализе, включенном в Европейский позиционный документ по управлению ООО, который включал 29 исследований и 2751 пациента. Напротив, чувствительность и специфичность ТТЭ ( трансторакальная эхокардиография, ЭХОКГ) составили 82% и 92%. Исследование, представленное в 2022 году на Международной конференции по инсульту и Европейской конференции по инсульту, сравнивало роботизированную ТКД (raTCD), выполненную неподготовленным персоналом, с обычной ТКД у 129 пациентов (90% с острым инсультом). Первичной конечной точкой было обнаружение шунта справа налево. raTCD выявил 63,6% шунтов по сравнению с 20,9% в группе стандартного лечения . raTCD также выявил более высокую долю крупных шунтов (27% против 10%), чем в группе стандартного лечения. Использование raTCD является многообещающим, и его диагностическая эффективность должна быть дополнительно проверена в более крупных проспективных исследованиях.
Эхокардиография (ЭХОКГ)
TEE (тансэзофагальная, чрезпищеводная эхокардиография) с инъекцией физиологического раствора с перемешиванием ( Баббл – тест, BUBBLE test ) является в настоящее время золотым стандартом для диагностики PFO ( OOO) у пациентов с инсультом, с взвешенной чувствительностью 89% по сравнению с аутопсией или осмотром во время операции на сердце. Благодаря техническим усовершенствованиям чувствительность трансторакальной эхокардиографии ( ЭХОКГ ) возросла за последние 30 лет с 51% (95% ДИ, 36%–55%) в период с 1991 по 2000% до 80% (95% ДИ, 74%–86%) в период с 2001 по 2020 год. Она остается стабильно выше 80% с 2011 года. Ложноположительные результаты могут возникать при наличии легочных артериовенозных фистул и должны учитываться, когда пузырьки определяются в левом предсердии после 3–5 циклов инъекции физиологического раствора с перемешиванием.
Магнитно-резонансная томография сердца
Хотя магнитно-резонансная томография сердца (CMRI) более чувствительна, чем трансторакальная эхокардиография и TEE для обнаружения нескольких кардиоэмболических источников (например, тромба левого желудочка), она работает значительно хуже, чем TEE для обнаружения шунтов справа налево. В недавнем метаанализе, включающем 5 исследований и 236 пациентов, CMRI показала 29,3% (95% ДИ, 23,6%–35,0%) выход обнаружения по сравнению с 53,7% (95% ДИ, 47,4%–59,9%) для TEE Несмотря на свою относительно низкую диагностическую ценность для PFO, CMRI все еще может быть полезна для понимания роли моделей потока правого предсердия в риске парадоксальной эмболии. Однако ее текущее использование остается исследовательским. Исследования с использованием 3D-скоростной кодированной CMRI (4D-поток) выявили отличительные паттерны правопредсердного потока у пациентов с криптогенным инсультом и PFO по сравнению со здоровыми контрольными лицами. Эти паттерны правопредсердного потока зависят от пространственного расположения верхней и нижней полой вены. CMRI может помочь определить характеристики PFO высокого риска и понять динамику правопредсердного потока, связанного с PFO, и их связь с парадоксальной эмболией.
Компьютерная томография сердца
PFO можно идентифицировать с помощью однофазной компьютерной томографии сердца (CCT). Однако чувствительность CCT хуже, чем TEE. По сравнению с TEE, чувствительность CCT для диагностики PFO в одноцентровом исследовании составила 85,3%, а специфичность 33,3%, с отрицательной прогностической ценностью 33%. Примечательно, что 1 из 7 пациентов с PFO, диагностированным с помощью TEE, были пропущены при компьютерной томографии сердца (КТ). Однофазная CCT выполняется в течение части сердечного цикла, обычно в конце систолы или середине диастолы. В исследовании, включающем 70 пациентов с инсультом и PFO, CCT полного цикла показала чувствительность и специфичность 89,4% и 92,3% по сравнению с TEE. Чувствительность однофазной CCT в том же исследовании составила всего 72,7%. Повышенная радиация при полноцикловой КТ по сравнению с однофазной КТ может ограничить возможность ее использования, в основном у молодых женщин (например, потенциальный риск рака молочной железы).
Использование ККТ также может способствовать пониманию патофизиологии парадоксальной эмболии. Исследование с использованием трехмерного анализа динамики вычислительной жидкости на КТ сердца выявило специфические для PFO паттерны потока в левом предсердии и количественно оценило время пребывания в левом предсердии, оценку стаза крови. Исследование сравнивало эти параметры у здоровых участников без PFO или фибрилляции предсердий (ФП), пациентов с PFO с криптогенным инсультом и без него, а также у лиц с хронической ФП. Пациенты с PFO имели специфический паттерн потока в левом предсердии с 2 вихревыми кольцами, исходящими из правой и левой легочных вен, и третьей струей, исходящей из PFO. Время пребывания было увеличено у пациентов с PFO по сравнению со здоровыми субъектами и было ниже у PFO, чем у пациентов с ФП. Кроме того, время пребывания было выше у пациентов с PFO с предшествующим криптогенным инсультом, чем у тех, у кого его не было. Эти результаты согласуются с предыдущими исследованиями, предполагающими, что шунтирование справа налево приводит к дисфункции левого предсердия , а закрытие PFO приводит к нормализации морфологии и функции левого предсердия . Трехмерный вычислительный анализ динамики жидкости может быть использован для исследования альтернативных механизмов инсульта (например, дисфункции левого предсердия) у пациентов с инсультом и PFO. Применение искусственного интеллекта может еще больше повысить его потенциальную применимость в режиме реального времени и может представлять интересную область для будущих исследований.
- Высокоинформативное исследование Транскраниальная допплерография с Баббл тест (ТКД Bubble test, bubble study ) на оборудовании премиум и экспертного класса можно провести
В ALCOR clinic, г. Днепр, улица Юлиуша Словацкого 1А.
Тел. +380678880677 / +38050888067